Неорганічні речовини клітини. вода
Всі наявні в клітині з'єднання можна розбити на дві групи: органічні та неорганічні.
Неорганічні речовини - це хімічні речовини, які не є органічними, тобто вони не містять вуглецю (крім карбідів, ціанідів, карбонатів, оксидів вуглецю та деяких інших сполук, які традиційно відносять до неорганічних).
 Вода (оксид водню, Н2О) - прозора рідина, яка не має кольору (в малому обсязі) і запаху. У твердому стані називається льодом або снігом, а в газоподібному - водяною парою. 71% поверхні Землі вкрито водою (океани, моря, озера, річки).
Вода (оксид водню, Н2О) - прозора рідина, яка не має кольору (в малому обсязі) і запаху. У твердому стані називається льодом або снігом, а в газоподібному - водяною парою. 71% поверхні Землі вкрито водою (океани, моря, озера, річки). Середній вміст води в клітинах складає 80% від їх загальної маси. Однак, в залежності від таксономічної і тканинної приналежності клітин, а також їх віку та стану утримання води може змінюватися в широких межах.
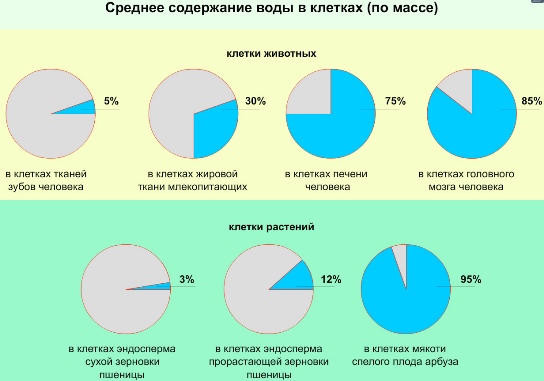
Вода - універсальне середовище живої матерії на клітинному рівні. У клітці вода знаходиться в двох формах: пов'язана (5%) - формує гідратів оболонки іонів і молекул, і вільна (95%) - бере участь в транспорті речовин цитоплазми.
165 років тому Гумбольт і Гей-Люссак довели, що 2 атома водню і атом кисню, з'єднуючись в молекулу, народжують воду.
Воді була дана чарівна влада стати соком життя на Землі. (Леонардо Да Вінчі)
Унікальні властивості води визначаються структурою її молекули
У молекулі води один атом кисню ковалентно пов'язаний з двома атомами водню. Позитивні заряди зосереджені у атомів водню в силу електронегативності кисню. Молекула являє собою диполь. Молекула води відчуває сильне електростатичне тяжіння, утворюючи водневі зв'язки з іншими молекулами.
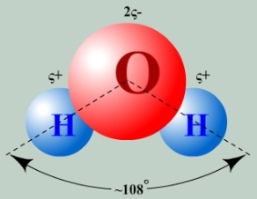 Молекула води має кутову форму: атоми водню по відношенню до кисню утворюють кут, рівний приблизно 108 °.
Молекула води має кутову форму: атоми водню по відношенню до кисню утворюють кут, рівний приблизно 108 °.
У молекулі води один атом кисню ковалентно пов'язаний з двома атомами водню. Через великий різниці електронегативності атомів водню і кисню електрони всіх атомів, що складають молекулу води, сильно зміщені в бік кисню. Внаслідок цього атом кисню набуває частковий негативний заряд. Тому молекула води - диполь: та частина молекули, де знаходиться водень, заряджена позитивно, а частина, де знаходиться кисень, - негативно.
Фізичні та хімічні властивості води багато в чому обумовлені наявністю водневих зв'язків між молекулами води - диполями.
властивості води
У рідкої воді поряд зі звичайними молекулами Н2О містяться асоційовані молекули, т. Е. З'єднані в більш складні агрегати (Н2О) x завдяки освіті водневих зв'язків. З підвищенням температури водневі зв'язки розриваються, і повний розрив настає при переході води в пару.
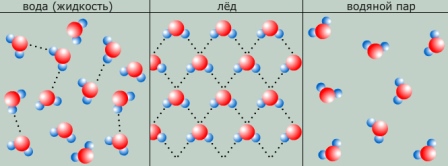
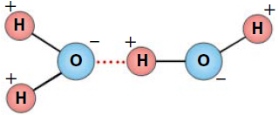 Наявністю водневих зв'язків між молекулами води пояснюються аномалії її фізичних властивостей:
Наявністю водневих зв'язків між молекулами води пояснюються аномалії її фізичних властивостей:
- висока температура і теплота плавлення і кипіння (в порівнянні з сполуками водню з схожим молекулярною вагою);
- висока теплоємність і низька в'язкість рідкої води;
- аномальне теплове розширення при замерзанні (при нагріванні від 0 до 4 ° C вода стискається. Завдяки цьому можуть жити риби в замерзаючих водоймах коли температура падає нижче 4 ° C, більш холодна вода, як менш щільна, залишається на поверхні і замерзає, а під льодом зберігається позитивна температура);
- вода - майже універсальний розчинник. Це найпоширеніший амфотерний полярний розчинник на Землі. У воді можна розчинити велику кількість речовин, молекули або іони яких здатні виявляти кислотні та (або) основні властивості.
Вода має теплоємністю, тобто здатністю поглинати теплоту при мінімальній зміні власної температури. Висока теплоємність і теплопровідність води забезпечують регуляцію температури організму, оберігаючи клітку від різких коливань температур.
Вода володіє великою теплотою випаровування. Випаровування супроводжується охолодженням, що обумовлює участь води в терморегуляції організму.
Завдяки своїй здатності утворювати слабкі хімічні зв'язки з іншими речовинами вода - прекрасний розчинник гідрофільних речовин. У вигляді іонів відбувається клітинний транспорт речовин. Всі речовини по відношенню до води діляться на гідрофільні і гідрофобні.
Гідрофільні речовини (грец. Hydor - вода і philia - любов) - речовини, добре розчинні у воді.
Гидрофильностью (хорошою смачиваемостью водою) мають речовини з іонними кристалічними гратами (оксиди, гідроксиди, силікати, сульфати, фосфати, глини і т. Д.), Речовини з полярними групами ОН, СООН, -NO 2 і ін.
 Гідрофобні речовини (грец. Hydor - вода і phobos - боязнь, страх) - речовини, не розчинні або погано розчинні у воді.
Гідрофобні речовини (грец. Hydor - вода і phobos - боязнь, страх) - речовини, не розчинні або погано розчинні у воді.
Гидрофобностью (поганий смачиваемостью) володіє більшість органічних речовин з вуглеводневими радикалами, метали, напівпровідники і т. Д.
Поняття гидрофильности і гідрофобності відносяться не тільки до тіл і речовин, у яких вони є властивістю поверхні, але і до окремих молекул, їх групам, атомам, іонів.
значення води
Вода забезпечує осмотичний надходження речовин в клітину, підтримує тургор, змінює щільність тканин.
Під дією деяких ферментів-каталізаторів вона вступає в реакції гідролізу, тобто в реакції, при яких до вільних валентності різних молекул приєднуються групи OH- або H + води. В результаті утворюються нові речовини з новими властивостями. Вміст води в організмі залежить від його віку та метаболічної активності.
Біологічна роль води в організмі
Роль Пояснення Розчинення Вода - універсальний амфотерний розчинник. Завдяки полярності, молекули взаємодіють з позитивно і негативно зарядженими іонами, сприяючи тим самим розчиненню речовин Продукт хімічних реакцій Молекули води вступають в хімічні реакції або є кінцевим продуктом реакцій в процесі обміну речовин Транспорт Надходження більшості речовин в клітку і видалення їх з клітки відбувається переважно у вигляді розчинів. Виділення розчинних продуктів обміну речовин з організму можливо тільки при достатній кількості води Терморегуляція Вода, як основний компонент живих організмів, бере участь в процесі терморегуляції завдяки здатності до повільного нагрівання і повільного охолодження. Вода, що виділяється ссавцями разом з потом, здійснює охолодження організму Підтримка пружності клітин і організмів Вода підтримує тургор клітин за рахунок осмотичного тиску. У організмів, які не мають скелетних утворень, пружні клітини і (або) порожнинна рідина формують гідроскелет
Вологолюбні представники флори яскраво-зеленого забарвлення (осока, очерет, перстач гусячий, мати-й-мачуха, кінський щавель, кропива, папороть) вважають за краще рости там, де грунтові води підходять близько до поверхні землі. Відшукати на місцевості водоносні жили, щоб не промахнутися з риттям колодязя, можна і за допомогою інших народних прикмет. Наприклад, давно помічено, що вишні і яблуні погано ростуть там, де грунтові води підходять близько до поверхні землі. А ось верба, верба, вільха, береза, навпаки, відчувають себе в таких місцях чудово.
Руді мурашки воду недолюблюють. У місцях, де вони влаштовують свої мурашники, копати криницю - справа майже безнадійна: до води не докопаєшся.
Про "живий" і "мертвої" воді
У народних казках часто зустрічаються сюжети про «живий» і «мертвої» води. Сучасна наука прийшла до висновку, що аналоги цих казкових речовин насправді існують. Це так звані «легка» і «важка» вода.
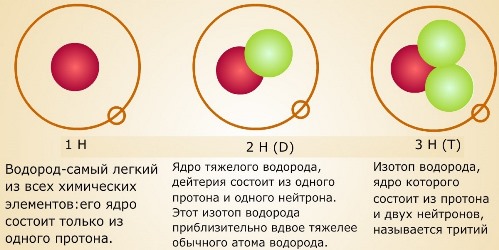
 Тридцяті роки ХХ століття були ознаменовані величезним проривом у фізиці елементарних частинок. У 1932 році російський фізик Дмитро Дмитрович Іваненко і німецький фізик Вернер Гейзенберг незалежно один від одного запропонували протонно-нейтронну модель ядра, згідно з якою ядро складається з позитивно заряджених протонів і не мають заряду нейтронів. Число протонів в ядрі відповідає числу нейтронів і одно зарядовому числу ядра. Відповідно до цієї теорії ізотопи - це різновиди атомів (і ядер) одного хімічного елемента з різною кількістю нейтронів в ядрі. У цьому ж 1932 році американським вченим Гарольдом Клейтоном Юрі був відкритий ізотоп водню дейтерій (D або ²H), а в 1934 році Ернестом Резерфордом - тритій (T або ³H).
Тридцяті роки ХХ століття були ознаменовані величезним проривом у фізиці елементарних частинок. У 1932 році російський фізик Дмитро Дмитрович Іваненко і німецький фізик Вернер Гейзенберг незалежно один від одного запропонували протонно-нейтронну модель ядра, згідно з якою ядро складається з позитивно заряджених протонів і не мають заряду нейтронів. Число протонів в ядрі відповідає числу нейтронів і одно зарядовому числу ядра. Відповідно до цієї теорії ізотопи - це різновиди атомів (і ядер) одного хімічного елемента з різною кількістю нейтронів в ядрі. У цьому ж 1932 році американським вченим Гарольдом Клейтоном Юрі був відкритий ізотоп водню дейтерій (D або ²H), а в 1934 році Ернестом Резерфордом - тритій (T або ³H).
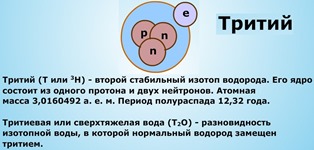 Займаючись подальшими дослідженнями, Юрі виявив, що ізотопи водню можуть входити до складу молекул води разом зі звичайними молекулами. Так була відкрита «важка вода». А в 1933 році Гілберт Льюїс отримав чистий тяжёловодородную воду.
Займаючись подальшими дослідженнями, Юрі виявив, що ізотопи водню можуть входити до складу молекул води разом зі звичайними молекулами. Так була відкрита «важка вода». А в 1933 році Гілберт Льюїс отримав чистий тяжёловодородную воду.
Таким чином, існують три різновиди води: звичайна чи легка (1H216O); дейтерієва або важка (D2O); тритієва або надважка (Т2О). Основну масу природної води - понад 99% - становить легка вода. Одна молекула важкої води доводиться на 3200 молекул легкої, а надважкої води у всій гідросфері одночасно налічується лише близько 20 кг. Однак чистої 1H216O в природних умовах не існує. У всьому світі така вода отримують в небагатьох спеціальних лабораторіях, шляхом багаторазового очищення природної води, або в результаті синтезу.
Різниться вода і за ізотопним складом кисню. Крім кисню 16O, в природі існують ще два природних ізотопу - 17O і 18O. У природних водах в середньому на кожні 10 тисяч атомів ізотопу 16O припадає 4 атома ізотопу 17O і 20 атомів ізотопу 18O. За сучасними даними число ізотопних різновидів води може досягати 135.
Важка вода застосовується в ядерних реакторах для гальмування нейтронів. А ось використання її для поливання рослин призводило до припинення їх росту. Ще більш невтішними були результати дослідів на тваринах: отримуючи важку воду у великих концентраціях, тварини гинули, коли половина води в їх тілі була дейтерированного. Однак деякі мікроорганізми добре себе почувають в 70% розчині D2O, а бактерії здатні жити навіть у чистій важкій воді.
«Легка вода», де дейтерій і важкий кисень відсутні або їх зміст значно знижено, навпаки, мають цілу низку корисних біологічних властивостей.
Експериментально були отримані результати: миші, що отримали значну дозу опромінення, мали більший термін життя, якщо вони пили легку воду. Крім того, експерименти показали, що «легка вода» уповільнює зростання деяких типів пухлин, стимулює зростання.
<Попередня сторінка "Хімічний склад клітини"
Наступна сторінка "Неорганічні речовини клітини. Мінеральні солі">
